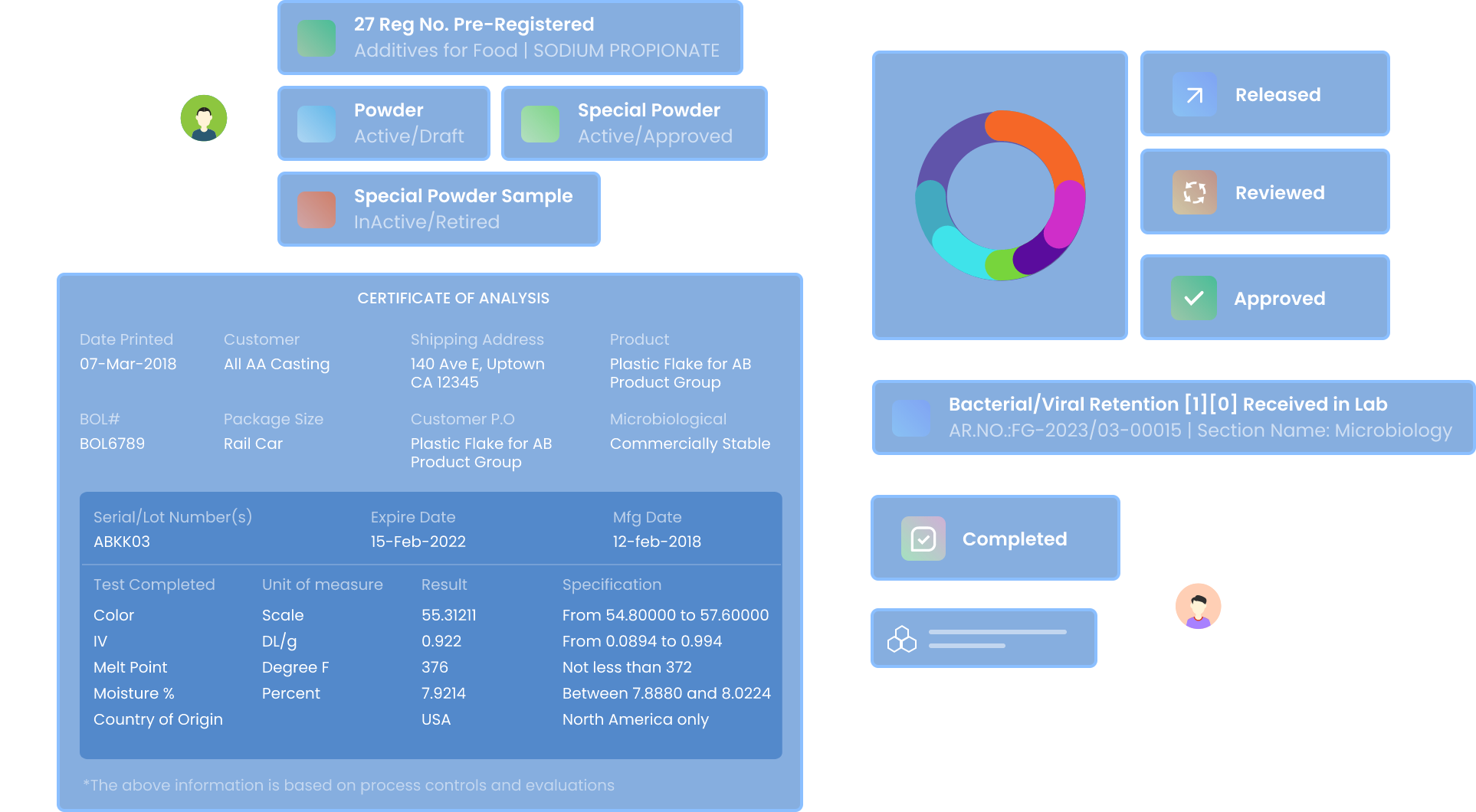
Flexible Probenregistrierung und -prüfung
Registrieren und prüfen Sie jede Art von Probe – Rohstoffe, Fertigprodukte, Patientenproben, Proben aus klinischen Studien oder Proben aus Forschungs- und Entwicklungsprojekten.
● Dynamische Vorlagen für die Probenregistrierung mit Drag-and-Drop-Feldern
● Versionskontrollierte Vorlagenverwaltung für Datenintegrität
● Verfolgung des Probenlebenszyklus mit vollständiger Metadatenerfassung
Kernfunktionen von LIMS
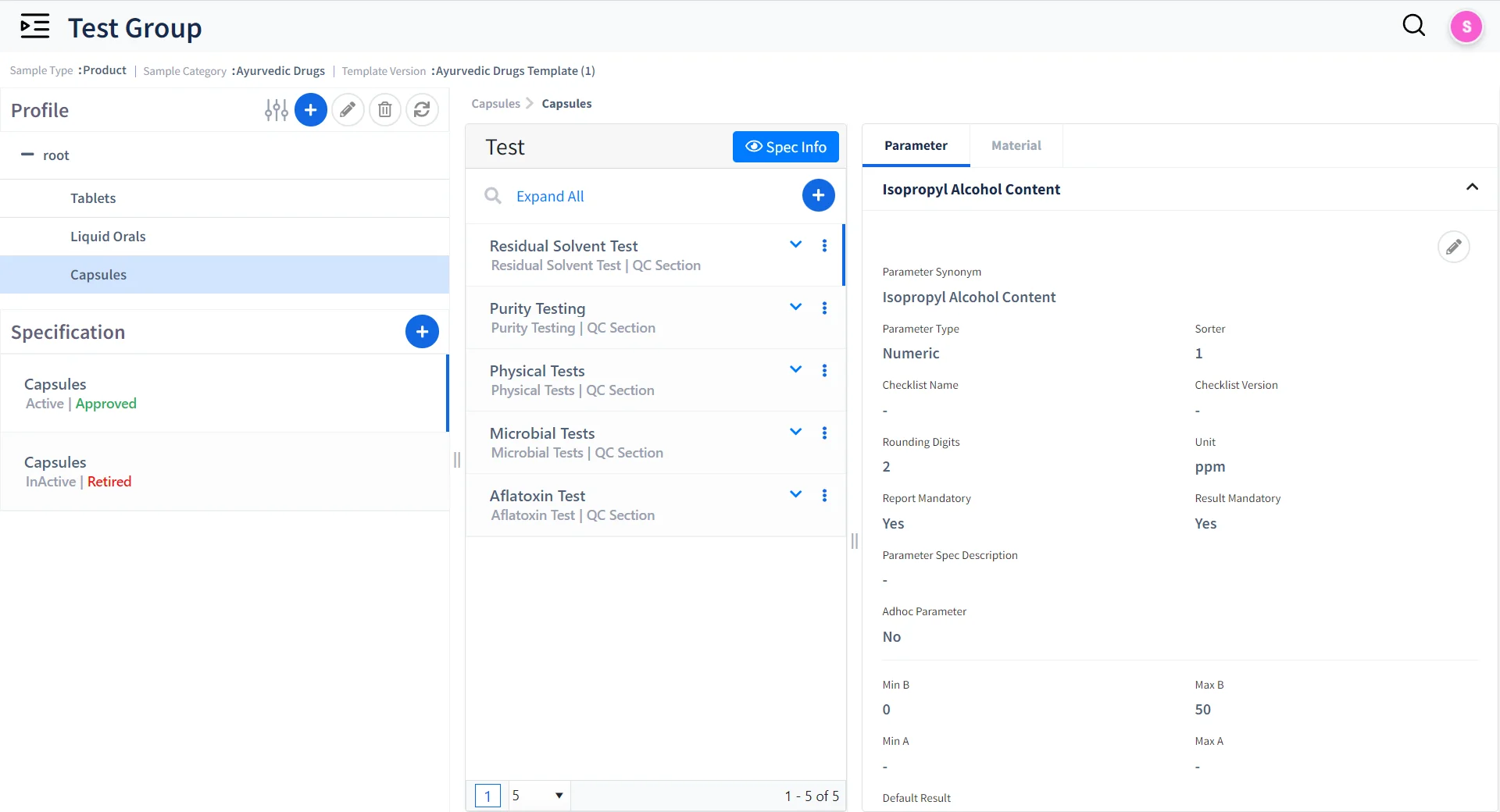
Einheitliches Test- und Spezifikationsmanagement
Testgruppen verwalten
Erstellen und verwalten Sie mehrere Testgruppen für Proben auf der Grundlage von Testparametern mit Probenmanagement-Software. .
Rückverfolgbarkeit gewährleisten
Verwalten Sie Testspezifikationen mit Versionskontrolle und Freigabekontrolle, um eine hohe Datenintegrität im Labor sicherzustellen.
Testspezifikationen definieren
Legen Sie Grenzwerte auf der Grundlage der erwarteten Testergebnisse fest, um Compliance und Konsistenz in der
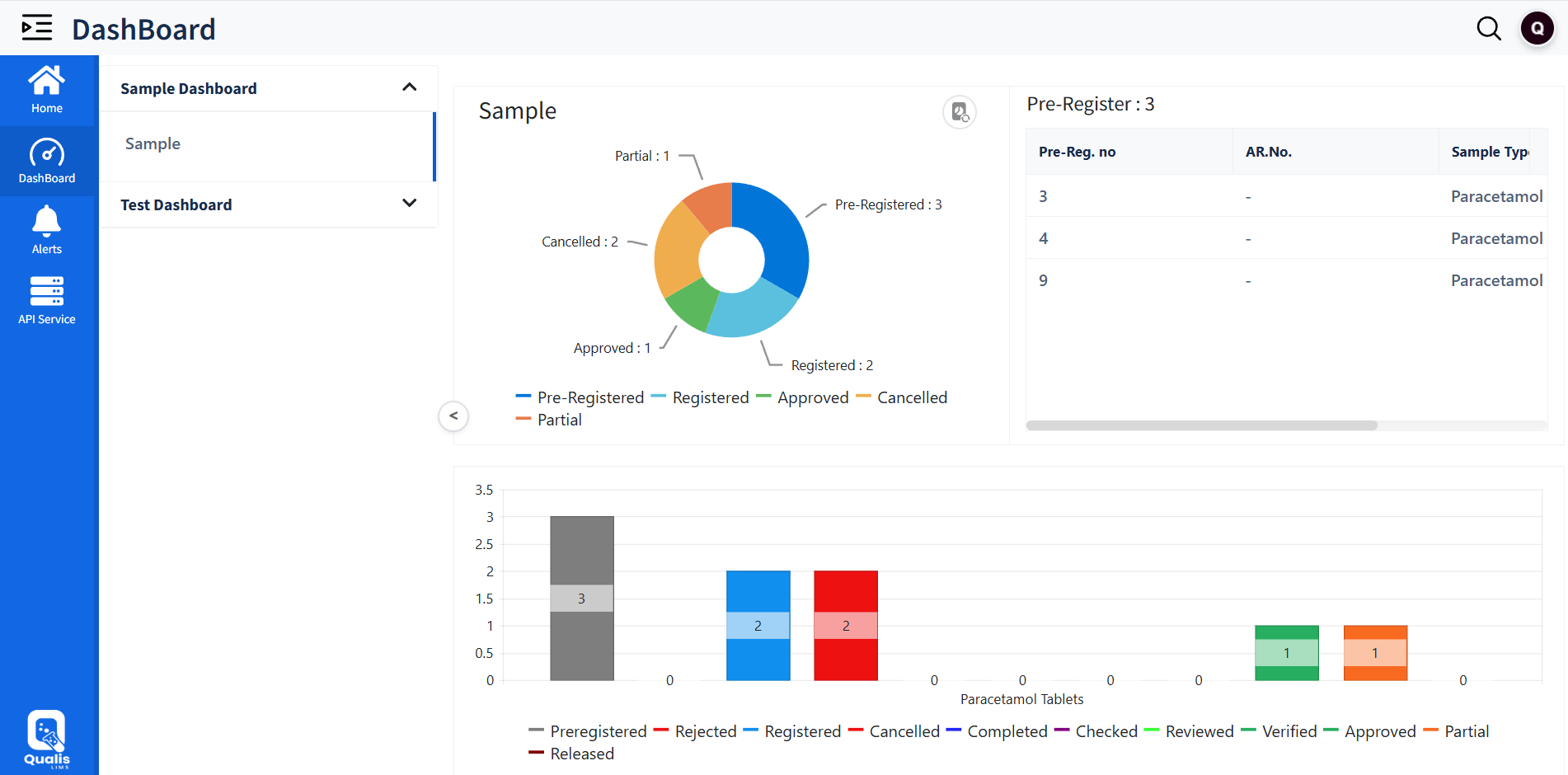
Live Dashboards und Warnmeldungen
Umfassendes Dashboard
für operative Transparenz und verbesserte Laborautomatisierung.
Intuitiv Warnmeldungen
für Genehmigungen, Kalibrierungsfristen, Arbeitsaufträge und Compliance-relevante Ereignisse, um Datenintegrität im Labor sicherzustellen.
Kontrollierte Sicht
für Manager, Analysten und Qualitätssicherung – optimiert durch moderne Laborsoftware für effizientes Monitoring.
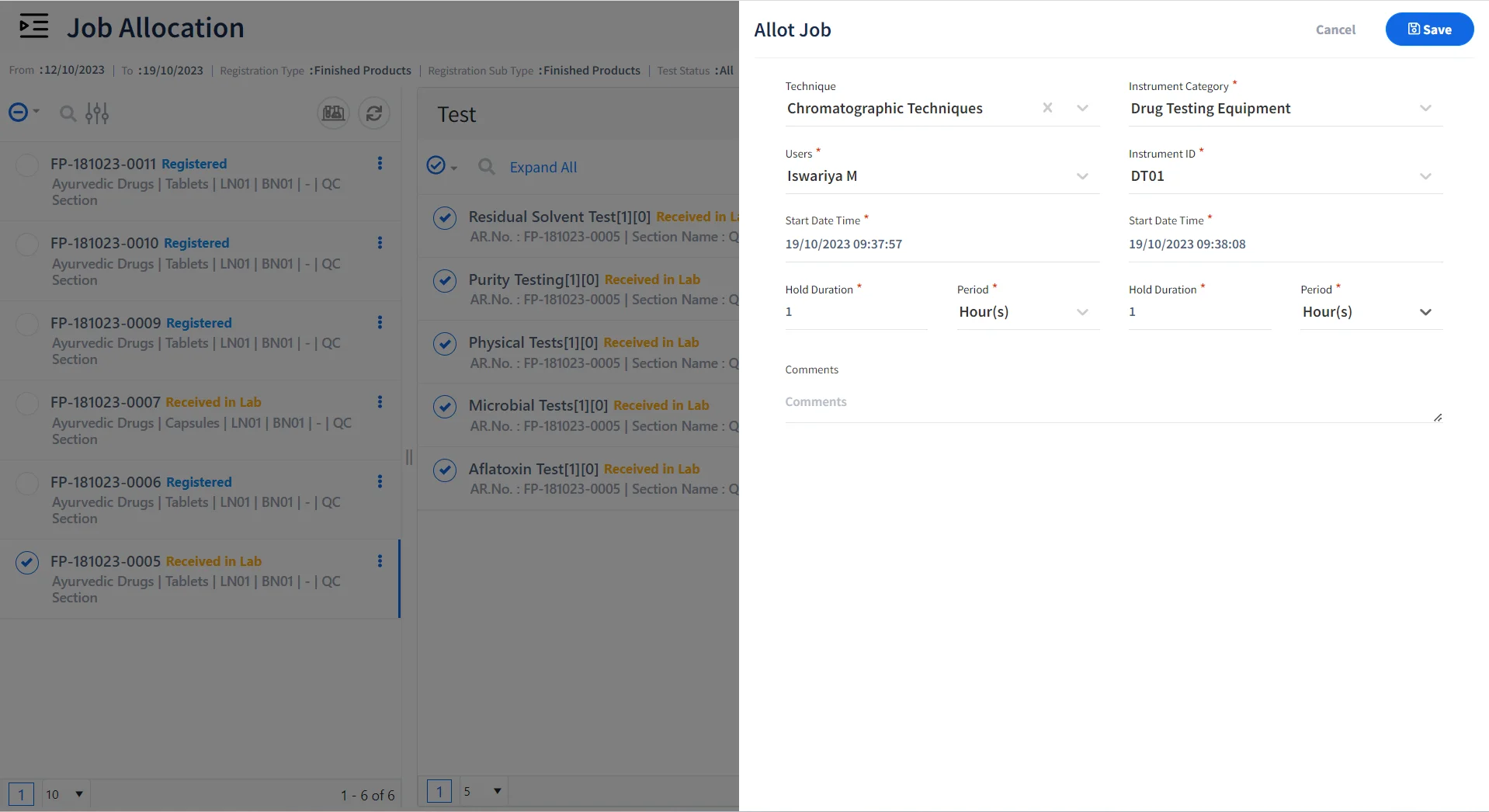
Zuweisung von Aufgaben an zertifiziertes Personal und qualifizierte Instrumente
Aufträge zuweisen
Weisen Sie Tests, Instrumente und zu testende Proben verschiedenen Mitarbeitern zu, um Laborabläufe zu automatisieren und die Effizienz im Labor zu steigern.
Rollenspezifische Aufgaben zuweisen
Weisen Sie Laborpersonal rollenbasierte Aufgaben für die Durchführung bestimmter Tests zu – unterstützt durch Laborsoftware mit rollenbasierter Zugriffskontrolle.
Tests zertifiziertem Personal zuweisen
Stellen Sie sicher, dass nur zertifiziertes Personal für spezifische Aufgaben oder Techniken verantwortlich ist, um Compliance und Datenintegrität im Labor zu gewährleisten.
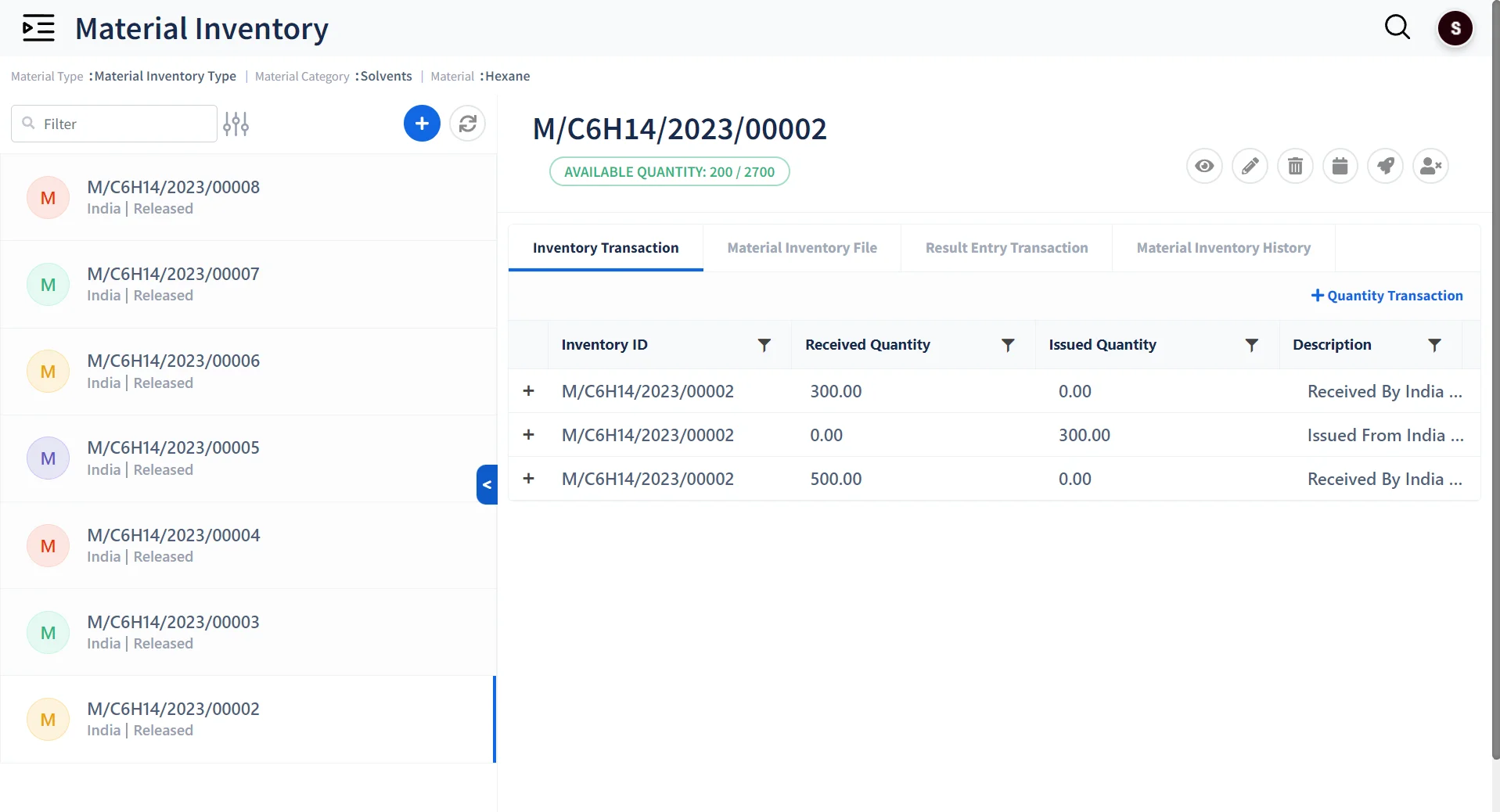
Standardisierte Bestandsverwaltung
Barcode-Etiketten zuweisen
Verwalten Sie mehrere Kategorien von Bestandsmaterialien mit Barcode-Etiketten über die Laborsoftware.
Barcode-Etiketten zuweisen
Erfassen und verfolgen Sie die Verwendung des Bestands innerhalb Ihres LIMS Software.
Optimieren Sie die Materiallagerung
Schaffen Sie dynamische Lagerstrukturen für die Lagerung von Materialien.
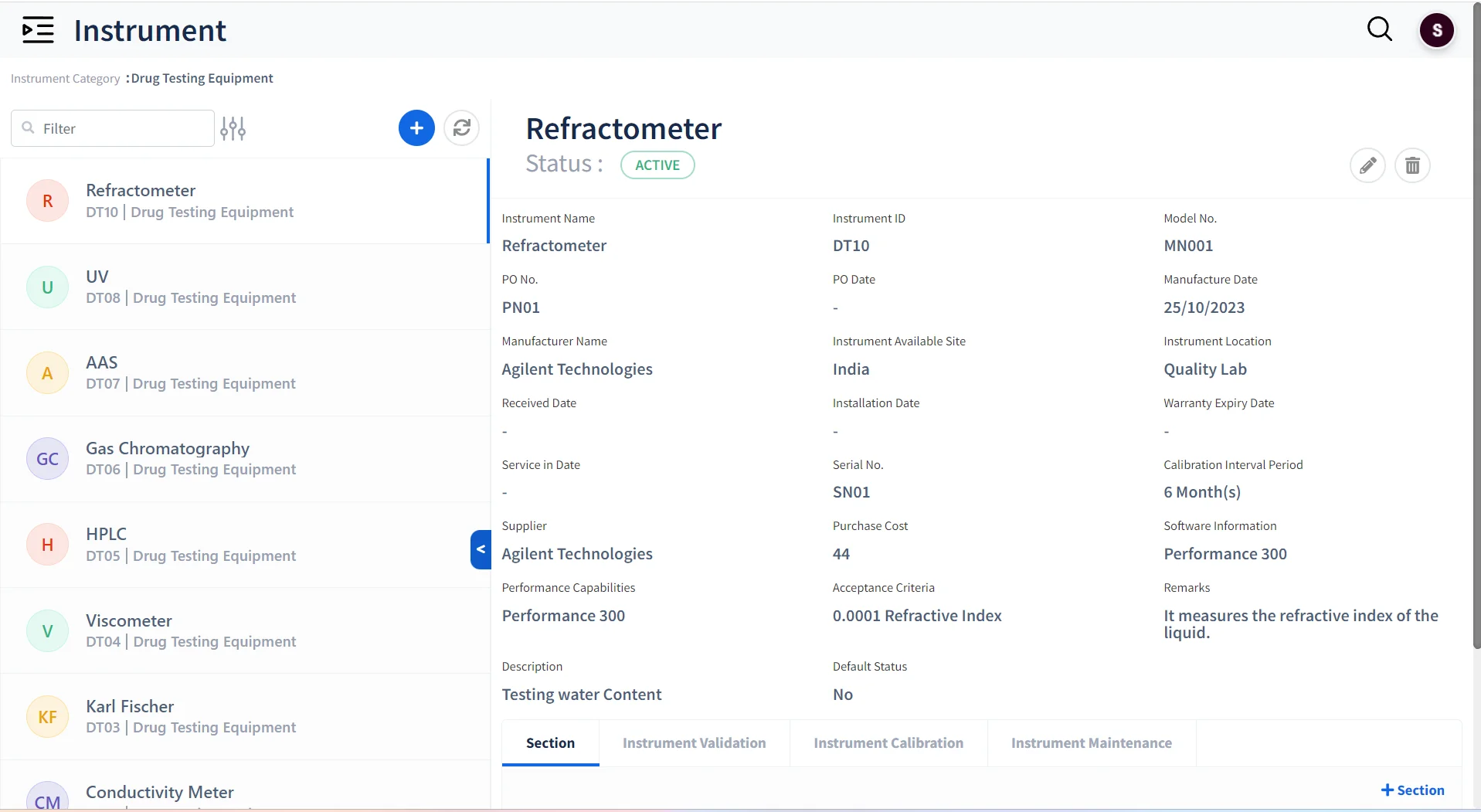
Instrumenten- und Geräteverwaltung
Verfolgung der Instrumentennutzung
Verwalten Sie alle im Labor eingesetzten Instrumente und Geräte.
Instrumentenprotokolle führen
Überwachen Sie Validierung, Kalibrierung und Wartung Ihrer Instrumente.
Zuverlässigkeit der Instrumente überprüfen
Stellen Sie sicher, dass ausschließlich kalibrierte Instrumente für Tests verwendet werden.
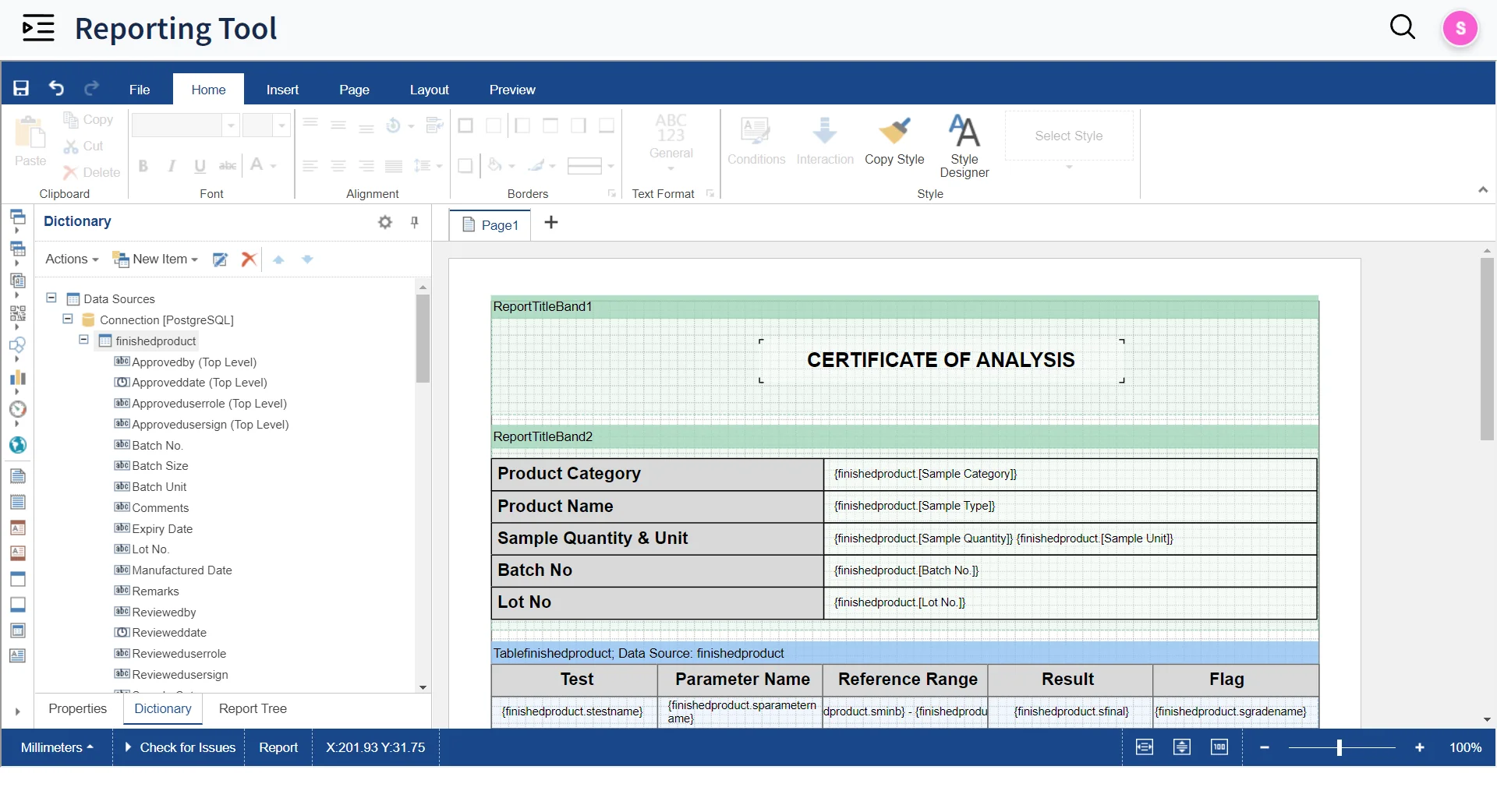
Automatisierte Eingabe von Ergebnissen und Berichterstellung
Berichtsvorlagen entwerfen
Erstellen Sie Vorlagen für Berichte mit dem integrierten Berichtstool und generieren Sie automatisch SQL-Abfragen mithilfe des Abfrage-Generators
Berichte bereitstellen
Stellen Sie Berichte über das Qualis-Portal für externe Stakeholder zur Verfügung.
Genehmigen und freigeben
Genehmigen und veröffentlichen Sie Berichte in Sekundenschnelle mit elektronischen und digitalen Signaturen.
Warum Qualis LIMS wählen

Webbasiert und plattformunabhängig
Chrome, Firefox, Safari etc

Hoch skalierbar
mehrere Standorte, mehrere Abteilungen, mehrere Labore

Compliance-fähig
21 CFR Part 11, EudraLex Anhang 11, ISO 17025, GLP, GAMP 4

Konfigurierbarkeit ohne Programmierung
Workflows ohne Programmierung anpassen

Geringere Compliance-Kosten
vorvalidierte Module und auditfähige Funktionen
Compliance und Audit-Bereitschaft
Entwickelt nach den ALCOA+-Prinzipien, mit Prüfpfaden, rollenbasierter Zugriffskontrolle und elektronischer Datensatzintegrität. Qualis LIMS hilft Teams dabei, für FDA-, EMA-, NABL- und ISO-Audits bereit zu sein, und minimiert den Vorbereitungsaufwand und den Dokumentationsaufwand.
Die wichtigsten Vorteile auf einen Blick

Vollständige Workflow-Automatisierung
von der Probenregistrierung bis zur Freigabe von Berichten

Integrierte Einhaltung gesetzlicher Vorschriften
21 CFR Part 11, ISO 17025, GLP, GAMP 4

Verbesserte Datenintegrität
ALCOA+, sichere Prüfpfade, granularer Zugriff

Schnellere Durchlaufzeiten (TAT)
Warnmeldungen, Dashboards, Probenuntersuchungen mit hohem Durchsatz

Skalierbar für jede Laborgröße
von einem Standort bis zu mehreren Standorten weltweit

Kostengünstige Bereitstellung
SaaS oder vor Ort mit geringem IT-Aufwand